Ароматические соединения. Ароматичность: критерии ароматичности, правило ароматичности Хюккеля, примеры бензоидных и небензоидных ароматических соединений Ароматические органические вещества

Арены (ароматические углеводороды) - соединения, в молекулах которых содержится одно или несколько бензольных колей - циклических групп атомов углерода со специфическим характером связей.
Бензол - молекулярная формула С 6 Н 6 . Впервые была предложена А. Кекуле:
Строение аренов.
Все 6 атомов углерода находятся в sp 2 -гибридизации . Каждый атом углерода образует 2 σ -связи с двумя соседними атомами углерода и одним атомом водорода, которые находятся в одной плоскости. Углы составляют 120°. Т.е. все атомы углерода лежат в одной плоскости и образуют шестигранник. У каждого атома есть негибридная р -обиталь, на которой находится неспаренный электрон. Эта орбиталь перпендикулярна плоскости, и поэтому π -электронное облако «размазано» по всем атомам углерода:

Все связи равноценны. Энергия сопряжения - количество энергии, которую надо затратить, чтобы разрушить ароматическую систему.
Именно это обуславливает специфические свойства бензола - проявление ароматичности. Это явление было открыто Хюккелем, и называется правилом Хюккеля.
Изомерия аренов.
Арены можно разделить на 2 группы:
- производные бензола:

- конденсированные арены:

Общая формула аренов - С n H 2 n -6 .
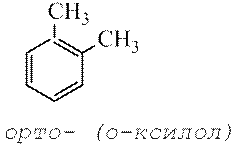
Для аренов характерна структурная изомерия, которая объясняется взаимным расположением заместителей в кольце. Если в кольце находится 2 заместителя, то они могут находиться в 3-х различных положениях - орто (о-), мета (м-), пара (п-):

Если от бензола «отобрать» один протон, то образуется радикал - C 6 H 5 , которое носит название арильного радикала. Простейшие:

Называют арены словом «бензол» с указанием заместителей в кольце и их положения:

Физические свойства аренов.
Первые члены ряда - жидкости без цвета с характерным запахом. Они хорошо растворяются в органических растворителях, но нерастворимы в воде. Бензол токсичен, но имеет приятный запах. Вызывает головную боль и головокружения, при вдыхании больших количеств паров можно потерять сознание. Раздражает слизистую оболочку и глаза.
Получение аренов.
1. Из алифатических углеводородов с помощью «ароматизации» предельных углеводородов, входящих в состав нефти. При пропускании над платиной или оксидом хрома наблюдается дигидроциклизация:

2. Дегидрирование циклоалканов:

3. Из ацетилена (тримеризация) при пропускании над раскаленным углем при 600°С:

4. Реакция Фриделя - Крафтса в присутствии хлорида алюминия :

5. Сплавление солей ароматических кислот с щелочью:
Химические свойства аренов.
Реакции замещения аренов.
Ядро аренов обладает подвижной π -системой, на которую действуют электрофильные реагенты. Для аренов характерно электрофильное замещение, которое можно представить так:

Электрофильная частица притягивается к π -системе кольца, затем образуется прочная связь между реагентом Х и одним из атомов углерода, при этом единство кольца нарушается. Для восстановления ароматичности выбрасывается протон, а 2 электрона С-Н переходят в π-систему кольца.
1. Галогенирование происходит в присутствии катализаторов - безводных хлоридов и бромидов алюминия , железа :

2. Нитрование аренов. Бензол очень медленно реагирует с концентрированной азотной кислотой при сильном нагревании. Но если добавить серную кислоту , то реакция протекает очень легко:
3. Сульфирование протекает под воздействием 100% - серной кислоты - олеума:
4. Алкилирование алкенами . В результате происходит удлинение цепи, реакция протекает в присутствии катализатора - хлорида алюминия:
Реакции присоединения аренов.
1. Гидрирование (при катализаторах) аренов:

2. Радикальное галогенирование при взаимодействии паров бензола и сильного УФ-излучения. В результате образуется твердый продукт - С 6 H 6 Cl 6 :

3. Окисление кислородом воздуха. Реакция протекает при оксиде ванадия (V) и 400°С:

Гомологи бензола имеют ряд отличий - на их продукты я изначальный заместитель в кольце:
Замещение в кольце возможно только в присутствие катализатора (хлорида железа и алюминия), замещение протекает в орто- и пара- положения по отношению к алкильному радикалу:

Если действуют сильные окислители (перманганат калия), то цепь алкильная разрушается и образуется бензойная кислота:


Дополнительные материалы по теме: Арены. Свойства аренов.
Химия 7,8,9,10,11 класс, ЕГЭ, ГИА |
|
| Основная информация по курсу химии для обучения и подготовки в экзаменам, ГВЭ, ЕГЭ, ОГЭ, ГИА | |
АРОМАТИЧНОСТЬ – сочетание определенных свойств, присущих большой группе соединений, называемых, соответственно, ароматическими.
Термин «ароматичность» ввел в 1865 Ф.Кекуле , установивший строение бензола и предложивший для него формулу:
Название «ароматический» связано с тем, что среди производных бензола существуют соединения с приятным запахом (например, нитробензол имеет запах миндаля).
Кекуле обратил внимание на то, что двойные связи в бензоле и в его производных заметно отличаются по свойствам от двойных связей в большинстве ненасыщенных соединений. Для бензола оказались крайне затруднены реакции присоединения (например, галогенов) по двойным связям, которые в случае ненасыщенных соединений проходят достаточно легко.
Кроме того, обнаружилось, что орто -дихлорбензол (атомы хлора находятся у двух соседних атомов углерода) не имеет изомеров, которые можно было ожидать на основе предложенной для него структурной формулы, где два атома хлора расположены либо у простой, либо у двойной связи:
В результате Кекуле предложил назвать связи в бензоле осциллирующими, то есть колеблющимися. Со временем это предположение получило дальнейшее развитие, и было усовершенствовано.
Наиболее характерны для бензола реакции замещения атомов водорода. Изучение химии бензола показало, что замена атома водорода на какую-либо группу определенным и, главное, предсказуемым образом влияет на реакционную способность остальных атомов водорода.
Если в бензольное ядро ввести группу, оттягивающую электроны от ядра (например, метильную), то последующее галогенирование приводит к замещению в орто- и пара- положении. При введении электроноподающей группы (например, карбоксильной) галоген направляется в мета -положение:
Долгое время ароматичностью считали набор указанных химических свойств, но постепенно были найдены более точные признаки, основанные на особенностях строения ароматических соединений.
Электронное строение бензола и родственных ему соединений в современном понимании выглядит следующим образом. В образовании двойных связей участвуют р -электроны атомов углерода, орбитали (область наиболее вероятного расположения электрона в пространстве) этих электронов имеют форму объемных восьмерок. В случае бензола орбитали взаимоперекрываются, образуя кольцевые орбитали, на которых располагаются все р -электроны молекулы:

В результате появляется единая замкнутая электронная оболочка, система приобретает высокую стабильность. Фиксированные простые и двойные связи в бензоле отсутствуют, все связи С–С усреднены и эквивалентны, поэтому чаще для обозначения ароматичности используют кольцевой символ, помещенный внутри цикла:
В образовавшихся циклических орбиталях возникает кольцевой ток, который может быть обнаружен специальными измерениями, дополнительно указывающими на ароматичность соединения.
Ароматичностью обладают плоские циклические молекулы, при этом количество электронов (m ), объединенных в единую циклическую систему, должно соответствовать правилу Хюккеля:
m = 4n + 2 (n = 0, 1, 2, 3...), n – число натурального ряда
Ниже показаны первые три представителя этого ряда ароматических молекул, соответствующие правилу Хюккеля: катион циклопропена , бензол и нафталин.
Расширение понятия «ароматичность» позволило применить этот термин к соединениям небензольного типа, но обладающим в то же время набором структурных и химических признаков, характерных для производных бензола.
В некоторых соединениях, где в состав цикла входят атомы O, S или N, например, в фуране, тиофене, пирроле так же, как в бензоле, существует устойчивая – в соответствии с правилом Хюккеля – шестиэлектронная замкнутая система. Четыре р- электрона (отмечены на рисунке синим цветом) предоставляют двойные связи цикла, а два s- электрона (отмечены красным цветом) дают атомы кислорода, серы или азота, имеющие неподеленную пару электронов.
Михаил Левицкий
Каждый вопрос экзамена может иметь несколько ответов от разных авторов. Ответ может содержать текст, формулы, картинки. Удалить или редактировать вопрос может автор экзамена или автор ответа на экзамен.
Ароматические соединения (арены) -- циклические органические соединения, которые имеют в своём составе ароматическую систему связей. Они могут иметь насыщенные или ненасыщенные боковые цепи.
К наиболее важным ароматическим углеводородам относятся бензол С6Н6 и его гомологи: толуол С6Н5СН3, ксилол С6Н4(СН3)2 и др.; нафталин C10H8, антрацен С14Н10 и их производные. Отличительные химические свойства -- повышенная устойчивость ароматического ядра и склонность к реакциям замещения. Основным источником получения ароматических углеводородов служат каменноугольная смола, нефть и нефтепродукты. Большое значение имеют синтетические методы получения. Ароматические углеводороды -- исходные продукты для получения кетонов, альдегидов и кислот ароматического ряда, а также многих других веществ.
Существуют также гетероциклические арены, среди которых чаще всего встречаются в чистом виде и в виде соединений -- пиридин, пиррол, фуран и тиофен, индол, пурин, хинолин.
Бензол и его гомологи сами являются хорошими растворителями для многих органических веществ. Все ароматические углеводороды нерастворимы в воде и хорошо растворимы в большинстве органических растворителей: многие из них хорошо перегоняются с водяным паром.
1. Ароматические углеводороды (арены)
ароматический углеводород
Ароматическими соединениями обычно называют карбоциклические соединения, в молекулах которых имеется особая циклическая группировка из шести углеродных атомов - бензольное ядро. Простейшим веществом, содержащим такую группировку, является углеводород бензол; все остальные ароматические соединения этого типа рассматривают как производные бензола.
Благодаря наличию в ароматических соединениях бензольного ядра они по некоторым свойствам значительно отличаются от предельных и непредельных алициклических соединений, а также и от соединений с открытой цепью. Отличительные свойства ароматических веществ, обусловленные наличием в них бензольного ядра, обычно называют ароматическими свойствами, а бензольное ядро - соответственно ароматическим ядром.
Следует отметить, что само название “ароматические соединения” теперь уже не имеет своего первоначального прямого значения. Так были названы первые изученные производные бензола, потому что они обладали ароматом или же были выделены из природных ароматических веществ. В настоящее же время к ароматическим соединениям относят многие вещества, обладающие и неприятными запахами или совсем не пахнущие, если в его молекуле содержится плоское кольцо с (4n + 2) обобщенными электронами, где n может принимать значения 0, 1, 2, 3 и т.д., - правило Хюккеля.
Ароматические углеводороды ряда бензола
Первый представитель ароматических углеводородов - бензол - имеет формулу C6H6 . Это вещество было открыто М.Фарадеем в 1825 г. В жидкости, образующейся при сжатии или охлаждении т.н. светильного газа, который получается при сухой перегонке каменного угля. Впоследствии бензол обнаружили (А.Гофман, 1845г.) в другом продукте сухой перегонки каменного угля - в каменноугольной смоле. Он оказался весьма ценным веществом и нашел широкое применение. Затем было установлено, что очень многие органические соединения являются производными бензола.
Первая структура бензола была предложена в 1865г. немецким ученым А. Кекуле:
Эта формула правильно отражает равноценность шести атомов углерода, однако не объясняет ряд особых свойств бензола. Например, несмотря на ненасыщенность, бензол не проявляет склонности к реакциям присоединения: он не обесцвечивает бромную воду и раствор перманганата калия, т. е. не дает типичных для непредельных соединений качественных реакций.
Особенности строения и свойств бензола удалось полностью объяснить только после развития современной квантово-механической теории химических связей. По современным представлениям все шесть атомов углерода в молекуле бензола находятся в sp2-гибридном состоянии. Каждый атом углерода образует s -связи с двумя другими атомами углерода и одним атомом водорода, лежащие в одной плоскости. Валентные углы между тремя s -связями равны 120°. Таким образом, все шесть атомов углерода лежат в одной плоскости, образуя правильный шестиугольник (s -скелет молекулы бензола).
Каждый атом углерода имеет одну негибридизованную р-орбиталь. Шесть таких орбиталей располагаются перпендикулярно плоскому s -скелету и параллельно друг другу (рис. а). Все шесть электронов взаимодействуют между собой, образуя p -связи, не локализованные в пары как при образовании двойных связей, а объединенные в единое p -электронное облако. Таким образом, в молекуле бензола осуществляется круговое сопряжение. Наибольшая p -электронная плотность в этой сопряженной системе располагается над и под плоскостью s -скелета (рис. б).
В результате все связи между атомами углерода в бензоле выровнены и имеют длину 0,139нм. Эта величина является промежуточной между длиной одинарной связи в алканах (0,154нм) и длиной двойной связи в алкенах (0,133 им). Равноценность связей принято изображать кружком внутри цикла (рис. в). Энергия образования молекулы бензола, рассчитанная исходя из наличия трех простых связей С-С, трех двойных и шести связей С-Н, равна 5355кДж/моль. Круговое сопряжение дает выигрыш в энергии 150 кДж/моль. Эта величина составляет энергию сопряжения -- количество энергии, которое нужно затратить, чтобы нарушить ароматическую систему бензола.
Такое электронное строение объясняет все особенности бензола. Бензол трудно вступает в реакции присоединения, т.к. это привело бы к нарушению сопряжения. Такие реакции возможны только в очень жестких условиях.
В 1931 г. Хюккель на основании квантово-механических расчетов сформулировал правило, гласящее, что соединение должно проявлять ароматические свойства, если в его молекуле содержится плоское кольцо с (4n+2) обобщенными электронами, где n может принимать значения 1,1,2,3 и т.д. Согласно этому правилу, системы, содержащие 6,10,14 и т.д. обобщенных электронов, являются ароматическими. Примерами таких углеводородов могут служить бензол(n=1), нафталин (n=2) и антрацен (n=3).
Антрацен Нафталин
Под ароматичностью понимают способность некоторых предельных соединений легко вступать в реакции замещения, а не присоединения и устойчивость к действию окислителей, температуры и т.п. Это понятие сформировалось в результате изучения свойств соединений ряда бензола, в частности углеводородов состава CnH2n-6, которые, несмотря на формальную ненасыщенность, легко вступают в реакции замещения и устойчивы по отношению к окислителям.
2. Номенклатура и изомерия
Условно арены можно разделить на два ряда. К первому относят производные бензола (толуол или дифенил), ко второму -- конденсированные арены (простейший из них -- нафталин):
Гомологический ряд бензола отвечает общей формуле С6Н2n-6.
Структурная изомерия в гомологическом ряду бензола обусловлена взаимным расположением заместителей в ядре. Монозамещенные производные бензола не имеют изомеров положения, так как все атомы в бензольном ядре равноценны. Дизамещенные производные существуют в виде трех изомеров, различающихся взаимным расположением заместителей.
Положение заместителей указывают цифрами или приставками: орто- (о-), мета- (м-), пара- (п-). Радикалы ароматических углеводородов называют арильными радикалами. Радикал С6Н5 -- называется фенил.
3. Физические свойства
Низшие члены гомологического ряда бензола представляют собой бесцветные жидкости с характерным запахом. Плотность и показатель преломления у них значительно выше, чем у алканов и алкенов. Температура плавления заметно выше, особенно у конденсированных многоядерных углеводородов (табл.). Из-за высокого содержания углерода все ароматические соединения горят сильно коптящим пламенем. Бензол и его гомологи сами являются хорошими растворителями для многих органических веществ. Все ароматические углеводороды нерастворимы в воде и хорошо растворимы в большинстве органических растворителей: многие из них хорошо перегоняются с водяным паром.
Химические свойства
Бензол, несмотря на то, что по составу он является ненасыщенным соединением, проявляет склонность преимущественно к реакциям замещения, и бензольное ядро очень устойчиво. В этом заключаются свойства бензола, которые называют ароматическими свойствами. Последние характерны и для других ароматических соединений; однако различные заместители в бензольном ядре влияют на его устойчивость и реакционную способность; в свою очередь бензольное ядро оказывает влияние на реакционную способность соединенных с ним заместителей. Рассмотрим следующие группы реакций ароматических углеводородов: а) реакции замещения, б) реакции присоединения и в) действие окислителей.
Реакции замещения. При замещении в бензольном кольце возможны три типа реакций в зависимости от природы атакующей частицы.
Радикальное замещение SR.
R.+H: С6Н5>R- С6Н5+ H.
Если атакующий реагент R.-радикал, несущий неспаренный электрон, то водород, связанный с атомом углерода ядра, отщепляется с одним из электронов электронной пары у-связи. Такой тип замещения называется радикальным. Реакция радикального замещения редко используется в ароматическом ряду.
Нуклеофильное замещение SN. При действии несущих отрицательный заряд нуклеофильных частиц на замещенный бензол С6Н5Х (где Х-заместитель) отщепляющаяся группа Х - уходит вместе с парой у -электронов, ранее осуществляющих ее связь с ядром:
Z-+ X: С6Н5> Z- С6Н5+Х-
Примером может служить реакция натриевой соли бензолсульфокислоты со щелочью. Эта реакция лежит в основе промышленного метода получения фенола:
Для успешного протекания реакций нуклеофильного замещения в ядре должен находится дополнительно один или лучше два сильных электроноакцепторных заместителя (-NO2, -SO3H ,-CF3)
Электрофильное замещение SE.
Все электрофилы являются кислотами Льюиса.
Общий вид реакций электрофильного замещения:
(катионный электрофил)
(нейтральный электрофил)
Во всех реакциях этого типа атакующий реагент (Y+) несет на атоме, вступающем в связь с углеродным атомом бензольного ядра, положительный заряд либо имеет ярко выраженный катионоидный характер и образует новую связь за счет пары электронов, ранее осуществлявшей связь С-Н. Замещающийся атом водорода уходит в виде протона:
Методы получения
Природные источники ароматических углеводородов. В промышленности ароматические углеводороды получают путем сухой перегонки каменного угля, а также из нефти.
Получение из каменного угля. Каменный уголь - один из наиболее ценных для народного хозяйства ископаемых продуктов, добываемых в огромных количествах. Используют каменный уголь как топливо и как сырье для получения многих важных продуктов. По составу каменный уголь - сложное органическое вещество; в процессе сухой перегонки, т.е. при нагревании в печах без доступа воздуха, при температуре 1000оС и выше, он разлагается и образуются следующие основные продукты: а) кокс (75-80 %); б) коксовый газ (до 3,5 %) и г) аммиачная вода (содержащая в основном неорганические вещества, главным образом аммиак).
Кокс - твердый продукт, представляющий собой углерод с некоторой примесью золы. Используется в металлургии как восстановитель, для выделения металлов, в основном железа, из руд (в доменном процессе). До начала второй половины XIX в. сухую перегонку каменного угля производили почти исключительно с целью получения кокса, поэтому этот процесс называют также процессом коксования угля.
Коксовый газ - побочный продукт коксования углей. Иначе его называют светильным газом, т.к. первоначально его использовали лишь как горючее, преимущественно для освещения. Основные составные части коксового газа - метан (30-50 %) и водород (30-50 %); кроме того, он содержит значительное количество паров ароматических углеводородов. Путем поглощения маслом с последующей отгонкой из коксового газа выделяют сырой бензол (до 1,5 % от веса угля) - смесь ароматических углеводородов с температурой кипения до 160оС. Из сырого бензола ректификацией получают чистый бензол, толуол, смесь ксилолов. Этим способом добывают основное количество бензола. Таким образом, в настоящее время коксовый газ - не только горючее, но и ценный источник ароматических соединений.
Каменноугольная смола (или каменноугольный деготь) - темная вязкая жидкость с неприятным запахом. До середины XIX столетия была бросовым продуктом коксования углей и ее подвергали уничтожению. Оказалось же, что она содержит множество ценнейших в практическом отношении ароматических соединений. Поэтому в настоящее время каменноугольную смолу подвергают тщательной переработке. Путем перегонки ее разделяют на следующие фракции: 1) легкое масло, tкип до 160 оС (до 2 %); 2) среднее масло, tкип 160-230 оС (до 12 %); 3) тяжелое или креозотовое масло, tкип230-270 оС (до 10 %); 4) антраценовое или зеленое масло, tкип 270-360 оС (до 23 %); 5) пек - остаток от перегонки (до 60 %).
Из легкого масла получают бензол, толуол, ксилолы; из среднего - нафталин, фенолы, пиридин; из тяжелого - в основном нафталин; из антраценового - антрацен, фенантрен и др. Пек - черная твердая масса, размягчающаяся при нагревании; применяется как строительный материал, для покрытия дорог и т.д.
1. Получение из алифатических углеводородов. При пропускании алканов с неразветвленной цепью, имеющих не менее шести атомов углерода в молекуле, над нагретой платиной или оксидом хрома происходит дегидроциклизация -- образование арена с выделением водорода:
2. Дегидрирование циклоалканов. Реакция происходит при пропускании паров циклогексана и его гомологов над нагретой платиной:
3. Получение бензола тримеризацией ацетилена по методу Н.Д. Зелинского:
4.Получение гомологов бензола по реакции Фриделя--Крафтса: типичное электрофильное замещение в ароматическом ядре; роль катализатора сводится к генерации атакующей частицы -- алкил- или ацилкатиона. Ниже рассмотрены примеры взаимодействия бензола с этилхлоридом и хлорангидридом уксусной кислоты:
C2H5CI + AlCl3 > C2H5+ + ?
C2H5+ + C6H6 > C6H5C2H5 + H+
CH3COCl + AlCl3 > CH3CO+ + ?
CH3CO+ + C6H6 > CH3COC6H5 + Н+
Н+ > HCl + AlCl3
5. Сплавление солей ароматических кислот со щелочью:
4. Механизм реакций электрофильного замещения в ароматическом ряду
Для соединений ароматического характера, имеющих замкнутую р- электронную систему, наиболее характерны реакции с электрофильными агентами. С помощью кинетических методов, что большинство реакций электрофильного замещения в ароматическом ряду протекает по двухстадийному механизму. На первой, медленной стадии происходит нарушение ароматической системы и переход атакуемого атома углерода в состоянии sp3-гибридизации:
Вторая, быстрая, стадия сопровождается восстановлением ароматической структуры и вследствие выигрыша энергии протекает легко и быстро:
Ar+ + В-> ArХ+ ВН
Протекание первой стадии обычно осуществляется с промежуточным образованием так называемого р-комплекса. р -комплексы представляют собой координационные соединения, в которых донором являются ароматические соединения, имеющие легко поляризуемые р- электроны, а акцепторами- галогены, галогеноводороды, сильные минеральные кислоты, безводные галогениды некоторых металлов и другие соединения, имеющие по разным причинам большое сродство к электронам.
р -комплексы не являются обычными химическими соединениями, в которых электрофильная частица связывается ковалентной связью с конкретным атомом реагирующего вещества. Они построены объемно, так как наибольшая р-электронная плотность ароматических соединений расположена по обе стороны бензольного кольца:
Во многих случаях р-комплексы удалось идентифицировать, чаще всего с помощью спектральных методов.
В отличие от р-комплексов у-комплесы представляют собой истинно химические соединения, в которых электрофильный агент Х+ образует ковалентную связь за счет двух р-электронов одной из связей бензольного кольца. В у-комплексе один из атомов углерода бензольного кольца переходит в состояние sp3- гибридизации, в котором все четыре связи направлены под углом 1090. При этом нарушается симметрия бензольного кольца, а группа Х+ и атом водорода оказываются выведенными из плоскости кольца:
Оставшиеся четыре р- электрона бензольного кольца равномерно распределяются между пятью атомами углерода, образуя «структуру циклопентадиенилкатиона». Эта структура менее устойчива, чем ароматическая.
Электронодонорные заместители, повышая электронную плотность в ароматическом ядре, увеличивают стабильность как р-, так и у-комплекса при электрофильном замещении.
Реакции электрофильного замещения завершаются отщеплением от у-комплекса протона и восстановлением ароматической системы. Этот процесс происходит при участии обладающего основными свойствами аниона В-, присутствующего в реакционной среде, и сопровождается выделением энергии:
Образование р- и у-комплесов зависит от ароматической структуры и от типа электрофильной частицы.
Нитрование. Бензол очень медленно реагирует с концентрированной азотной кислотой даже при сильном нагревании. Однако при действии так называемой нитрующей смеси (смесь концентрированных азотной и серной кислот) реакция нитрования проходит достаточно легко:
Галогенирование. При галогенировании ароматических соединений обычно применяют катализаторы (безводные АlСl3, FeСl3, АlВr3), вызывающие поляризацию или даже гетеролитическую диссоциацию молекулы галогена:
Положительный конец диполя атакует ароматические соединения, а отрицательный входит в состав комплекса с катализатором:
Алкилирование по Фриделю--Крафтсу. Алкилирование ароматических соединений обычно проводят галогеналкилами в присутствии хлорида алюминия.
В качестве алкилирующих агентов могут применяться также непредельные соединения и спирты в присутствии сильных минеральных кислот. В этом случае роль кислоты состоит в том, чтобы алкен или спирт перевести в соответствующий карбокатион:
При алкилировании первичными спиртами почти всегда наблюдается изомеризация углеродного скелета, что связано с перегруппировкой первичных карбокатионов в более устойчивые вторичные и третичные:
Ацилирование. Введение остатка кислоты RCO-. В качестве ацилирующих агентов используют галогенангидриды и ангидриды кислот. Катализатором обычно служит хлорид алюминия:
Механизм реакций нуклеофильного замещения в ароматическом ряду
Общепринятый механизм нуклеофильного замещения в ароматическом ряду включает двухстадийное протекание реакции аналогично тому, как и у электрофильного замещения. Первая стадия- атака нуклеофилом
Y- атома углерода, обычно связанного с заместителем, приводящая к образованию промежуточного у-комплекса:
В нем ароматическая система нарушена, так как тип гибридизации атома углерода в реакционном центре переходит из sp2 в sp3. На второй стадии отщепления Х- приводит к восстановлению ароматической системы, а результатом реакции является нуклеофильное замещение Х на Y.
Электроноакцепторные группы, находящиеся в бензольном ядре, такие, как NO2, NO, C? N, «объединяют» бензольное кольцо электронами, тем самым облегчая атаку бензольного кольца нуклеофильной частицей.
5. Реакционная способность ароматических соединений при электрофильном замещении
Молекула бензола симметрична, и все атомы углерода совершенно равноценны, поэтому электрофильная частица при образовании у-комплекса может атаковать с равной вероятностью любой из атомов углерода. В зависимости от природы заместителя при электрофильном замещении монозамещенных ароматических углеводородов могут образовываться три типа дизамещенные продуктов:
При сопоставлении имеющихся заместителей в бензольном ядре по их направляющему действию при атаке электрофильной частицы можно получить два ряда:
1) Группы, направляющие новый заместитель в орто- и пара- положения: ОН,NH2, NHR, NR2, OR, CH3, SH, SR, NHCOR-заместители Iрода, или орто-пара-ориентанты;
2) Группы, направляющие новый заместитель в мета- положение:NH3, NO2, SO3H, CHO, COR, COOH, COOR,CN- заместители II рода, или мета-ориентанты.
Cила ориентирующего влияния того или иного заместителя зависит от его положения в рядах. Наиболее сильные ориентанты занимают начало рядов, наиболее слабые - конец.
Замещение в производных бензола, содержащих ориентанты первого рода, идет легче, чем в самом бензоле. Замещение в производных бензола, содержащих заместитель второго рода, идет труднее, чем в самом бензоле. Сила этого влияния находится в такой же зависимости от положения заместителя в рядах, как и ориентирующее действие.
Любой заместитель взаимодействует с бензольным кольцом двояко: оказывает на него индуктивное влияние и может участвовать в сопряжении с бензольным кольцом. Индуктивное влияние и сопряжение приводят к значительному изменению электронной плотности на атомах углерода бензольного кольца.
Рассмотрим сначала производные бензола, содержащие заместители второго рода, например бензойную кислоту:
В этом случае атом углерода карбоксильной группы, непосредственно связанный с бензольным ядром, имеет пониженную электронную плотность (+у) за счет поляризации двойной связи С=О. Это Приводит к сдвигу у- электронов связи атома углерода ядра с этим заместителем по направлению от кольца, и такое индуктивное влияние вызывает общее «обеднение» ядра электронами и появление некоторого положительного заряда у всех атомов углерода бензольного кольца. Однако эффект сопряжения вследствие появления положительного заряда у+ на атоме углерода ядра, связанном с заместителем, действует таким образом, что наибольшее «обеднение» электронами наблюдается в о- и n- положениях (I). Сопряжение кратных связей заместителя с р- электронами бензольного кольца также приводит к смещению электронной плотности следующим образом (II):
Эффект сопряжения (-М-эффект) в данных случаях приводит к смещению р- электронов кратных связей в направлении к гетероатомам, имеющим кратные связи.
Из схемы видно, что обусловленный отрицательным индуктивным эффектом большой положительный заряд орто- и пара- атомов углерода еще более увеличивается, так как именно от этих атомов оттягиваются р- электроны вследствие отрицательного эффекта сопряжения, а в м-положениях электронная плотность несколько увеличивается. Так как атака электрофильной частицы идет по месту с наибольшей электронной плотностью. То в этом случае при реакции электрофильного замещения будут в первую очередь образовываться мета- изомеры.
По-другому должно быть распределение электронной плотности при наличии заместителя первого рода, например метильной группы:
Положительный индуктивный эффект метильной группы сообщает ядру бензола общую повышенную электронную плотность, причем за счет эффекта сопряжения наибольшую о- и n- положениях.
По-другому распределяется электронная плотность в том случае, когда заместителем является атом галогена (например, хлора). Как известно, хлор обладает отрицательным индуктивным эффектом. Этот -I- эффект вызывает общее обеднение бензольного кольца электронами (показано прямыми стрелками) появление частичного положительного заряда у всех атомов углерода, причем за счет эффекта сопряжения больше обедняются электронами о- и n- положения:
Однако атом хлора способен к проявлению слабого положительного эффекта сопряжения. Этот +М- эффект, действуя в противоположном направлении, приводит к некоторому повышению электронной плотности в о- и n- положениях. Поэтому замещение в первую очередь идет в о- и n- положения по отношению к атому галогена, но труднее, чем в незамещенном бензоле.
Третий типичный случай- наличие заместителя, обладающего слабым отрицательным индуктивным эффектом и большим положительным эффектом сопряжения. К таким заместителям относятся, например, группы ОН иNН2.
В молекулах фенола или анилина индуктивный эффект вызывает небольшую недостаточность электронной плотности на всех атомах углерода главным образом о- и n- положениях:
Однако сопряжение свободной электронной пары атома азота NH2- группы или атома кислорода ОН- группы приводит к значительному повышению электронной плотности в о- и n- положениях бензольного кольца:
Электрофильная атака будет идти в о- и n- положения и легче, чем в молекуле бензола.
При реакциях нуклеофильного замещения заместители оказывают противоположное ориентирующее действие, так как нуклеофильная частица атакует места с наименьшей электронной плотностью. В качестве примера можно привести реакцию гидроксилирования нитробензола:
6. Согласованная и несогласованная ориентация
Согласованная ориентация. При наличии в бензольном ядре двух заместителей их ориентирующее влияние может быть согласованным, когда они направляют третий заместитель в одно и то же положение. Это характерно для м-двузамещенных, в которых оба заместителя принадлежат к одному роду, и для о - и n- двузамещенных, содержащих заместители различных родов.
м-двузамещенных, в которых оба заместителя относятся ко второму роду (м-ориентанты), дают при введении третьего заместителя один изомер. Например, м - динитробензол может превратиться, правда в очень жестких условиях, в 1,3,5- тринитробензол:
В отличие от этого м-двузамещенные, содержащие заместители первого рода (о - и n-ориентанты), могут дать до трех изомеров (или если заместители в исходном соединении одинаковы, то два изомера). м-ксилол дает при нитровании два нитросоединения:
При нитровании м-крезола образуются три изомерных нитросоединения:
О-двузамещенные, содержащие заместители различных родов, также дают два изомера. Примером может служить о- нитротолуол. При хлорировании о- нитротолуола в качестве главного продукта образуется 6-хлор-2-нитротолуол и в меньшем количестве 4-хлор-2-нитротолуол:
Несогласованная ориентация. Имеются и такие двузамещенные бензолы, в которых один из заместителей направляет новые группы в иные положения, чем второй заместитель. Для этих соединений характерно наличие двух заместителей одного рода, находящихся в о- и n- положении друг к другу, или двух заместителей различных родов, расположенных в м- положении. В таких случаях несогласованной ориентации ориентирующие влияния конкурируют между собой, и в результате может образоваться много различных изомеров.
С образованием только одного изомера идет замещение в n- двузамещенных бензола с одинаковыми заместителями (например, в n- дихлорбензоле, n-ксилоле):
Соединения с одинаковыми заместителями в о-положении обычно образуют смесь двух изомеров. Например, при нитровании о- дихлорбензола получается как 3- нитро, так и 4- нитрозамещенное:
Если заместители обладают разной ориентирующей силой, то, как правило, ориентацию определяет более сильный ориентант (ОН- группа):
Если в молекуле бензола имеются заместители I B II родов, то ориентацию определяет в основном заместитель I рода.
9. Токсичность
При остром отравлении наблюдаются головная боль, тошнота, рвота, возбуждение, подобно алкогольному, затем постепенное угнетение, изредка судороги; смерть наступает от остановки дыхания. Для хронических отравлений характерны тяжелые поражения системы крови и кроветворных органов, сопровождающиеся снижением содержания в крови эритроцитов, лейкоцитов и тромбоцитов, расстройства функции нервной системы, поражения печени и органов внутренней секреции. Наиболее тяжелые хронические отравления вызывает бензол. При действии паров или пыли ароматических углеводородов наблюдается помутнение хрусталика. Раздражающее действие производных бензола на кожу возрастает по мере увеличения числа метильных групп, особенно выражено оно у мезитилена (триметилбензол). Замещение водорода в боковой цепи на галоген (хлор, бром) усиливает раздражающее действие ароматических углеводородов на дыхательные пути и слизистые оболочки глаз. Токсические свойства ароматических амино- и нитросоединений связаны с их способностью превращать оксигемоглобин в метгемоглобин.
Нафталин и его производные могут вызывать поражение нервной системы, желудочно-кишечного тракта, почек, раздражение верхних дыхательных путей и кожи. Соединениям многоядерных ароматических углеводородов с конденсированными кольцами присуща канцерогенная активность. Опухоли обычно возникают в местах непосредственного контакта с этими ароматическими углеводородами, но изредка и в отдаленных органах (мочевой пузырь)
10. Применение
Ароматические углеводороды играют важную роль в экономике с начала девятнадцатого столетия, когда в качестве растворителя каучука стал использоваться растворитель из каменноугольной смолы.
В настоящее время соединения ароматического ряда в чистом виде используются для синтеза пластмасс, синтетического каучука, красителей, взрывчатых веществ, пестицидов, детергентов, духов и лекарств. Эти вещества используются, главным образом, как компонент растворителей, и в разной пропорции входят в состав горючего.
Кумол используется как высокооктановая добавка к авиационному топливу, как разбавитель для эфироцеллюлозных красок и лаков, как важный исходный материал для синтеза фенола и ацетона, а также для крекингового получения стирола. Это вещество входит в состав многих промышленных нефтяных растворителей с температурой кипения от 150 до 160. Кумол хорошо растворяет жиры и смолы, и поэтому используется в качестве замены бензола во многих отраслях промышленности. п-цимол присутствует в некоторых эфирных маслах и может быть получен гидрированием моноциклических терпенов. Он является побочным продуктом производства бумаги из сульфитной целлюлозы и используется, в основном, совместно с другими растворителями и ароматическими углеводородами как разбавитель для лаков.
Кумарин применяется как дезодорирующий и усиливающий запах компонент в производстве мыла, табака, резиновых изделий и духов. Он также используется в фармацевтических препаратах.
Бензол запрещен к применению в товарах широкого потребления, а во многих странах было прекращено его использование в качестве растворителя и компонента жидкости для сухой химчистки. Бензол широко применялся при изготовлении стирола, фенолов, малеинового ангидрида и ряда детергентов, взрывчатых веществ, фармацевтических препаратов и красителей. Он использовался как топливо, химический реактив и экстрагирующий агент для семян и орехов. Моно-, ди- и триалкильные производные бензола используются, прежде всего, как растворители и разбавители в производстве духов и промежуточных материалов для красителей.
Эти вещества присутствуют в некоторых нефтепродуктах и в дистиллятах каменноугольной смолы. Псевдокумол используется при изготовлении духов, а 1,3,5-триметилбензол и псевдокумол используются также как промежуточные звенья в производстве красителей, но главное промышленное применение этих веществ - растворители и разбавители.
Толуол служит растворителем для масел, смол, натурального (в смеси с циклогексаном) и синтетического каучука, пеков, асфальта, дегтя и ацетилцеллюлозы (в горячей смеси с этиловым спиртом). Он служит растворителем и разбавителем для эфироцеллюлозных красок и лаков, а также растворителем чернил для гелиогравюры. Смешанный с водой, он образует азеотропные смеси, которые применяются для получения матовых поверхностей. Толуол входит в состав смесей, которые используются как чистящие средства во многих отраслях промышленности и в кустарных промыслах. Он используется при изготовлении детергентов и искусственной кожи, как важное сырье для органического синтеза, особенно для получения хлоридов бензоила и бензидена, сахарина, хлорамина, тринитротолуола и разнообразных красителей.
Нафталин используется как исходный продукт органического синтеза разнообразных химических соединений, как средство защиты от моли и компонент состава для защиты дерева. Его также используют при изготовлении индиго и применяют как наружное средство для уничтожения вшей у домашних животных и птицы.
Стирол широко применяется в производстве прозрачных пластмасс. Этилбензол используется как растворитель или разбавитель, компонент автомобильного и авиационного топлива, а также при производстве ацетата целлюлозы.
Заключение
Для аренов характерны реакции замещения. Наиболее важно электрофильное замещение: галогенирование, нитрование, сулъфирование, алкилирование и ацилирование по Фриделю-Крафтсу, нуклеофильное замещение.
Получают при каталитической дегидроциклизации алканов, то есть отщепление водорода с одновременной циклизацией. Реакция осуществляется при повышенной температуре с использованием катализатора, например оксида хрома.
Каталитическим дегидрированием циклогексана и его производных. В качестве катализатора используется палладиевая чернь или платина при 300 °C. (Н. Д. Зелинский)
Циклическим тримеризацием ацетилена и его гомологов над активированным углем при 600 °C. (Н. Д. Зелинский)
Алкилированием бензола галогенопроизводными или олефинами. (Реакция Фриделя -- Крафтса).
Все ароматические соединения -- твердые или жидкие вещества. Отличаются от алифатических и алициклических аналогов высокими показателями преломления и поглощения в близкой УФ и видимой области спектра. Все ароматические углеводороды нерастворимы в воде и хорошо растворимы в большинстве органических растворителей.
Соединения ароматического ряда в чистом виде используются для синтеза пластмасс, синтетического каучука, красителей, взрывчатых веществ, пестицидов, детергентов, духов и лекарств. Эти вещества используются, главным образом, как компонент растворителей, и в разной пропорции входят в состав горючего.
А РЕНЫ
Ароматические углеводороды (арены) – циклические углеводороды, объединяемые понятием ароматичности, которая обуславливает общие признаки в строении и химических свойствах.
Классификация
По числу бензольных колец в молекуле арены подразделяются на:
моноядерные
многоядерные

Номенклатура и изомерия
Структурным родоначальником углеводородов бензольного ряда служит бензол С 6 Н 6 от которого строятся систематические названия гомологов.
Для моноциклических соединений сохраняются следующие несистематические (тривиальные) названия:

Положение заместителей указывают наименьшими цифрами (направление нумерации не имеет значения),
|
|
|
а для ди замещенных соединений можно использовать обозначения орто, мета , пара.
|
|
|
|
Если в кольце три заместителя тони должны получить наименьшие номера, т.е. ряд «1,2,4» имеет преимущество перед «1,3,4».


1,2-диметил-4-этилбензол (верное название) 3,4-диметил-1-этилбензол (неверно)
Изомерия монозамещенных аренов обусловлена строением углеродного скелета заместителя, у ди- и полизамещенных гомологов бензола добавляется ещё изомерия, вызванная различным расположением заместителей в ядре.
Изомерия ароматических УВ состава С 9 Н 12:
|
|
|
|
|
Физические свойства
Температуры кипения и плавления у аренов выше, чем у алканов, алкенов, алкинов, малополярные, не растворимы в воде и хорошо растворимы в неполярных органических растворителях. Арены это жидкости или твердые вещества, имеющие специфические запахи. Бензолы и многие конденсированные арены токсичны, некоторые из них проявляют концерогенные свойства. Промежуточными продуктами окисления конденсированных аренов в организме являются эпоксиды, которые либо сами непосредственно вызывают рак, либо являются предшественниками канцерогенов.
Получение аренов
Многие ароматические УВ имеют важное практическое значение и производятся в крупном промышленном масштабе. Ряд промышленных способов основан на переработке угля и нефти.
Нефть состоит главным образом из алифатических и алициклических УВ, для превращения алифатических или ациклических УВ в ароматические разработаны способы ароматизации нефти, химические основы которых развиты Н.Д. Зелинским, Б.А. Казанским.
1. Циклизация и дегидрирование:
2. Гидродезметилирование:

3. Гомологи бензола получают путем алкилирования или ацилирования с последующим восстановлением карбонильной группы.
а) Алкилирование по Фриделю-Крафтсу:

б) Ацилирование по Фриделю-Крафтсу:

4. Получение бифенила по реакции Вюрца-Фитинга:
5. Получение дифенилметана по реакции Фриделя-Крафтса:
Строение и химические свойства.
Критерии ароматичности:
На основании теоретических расчетов и экспериментального изучения циклических сопряженных систем было установлено, что соединение ароматично, если оно имеет:
- Плоский циклический σ-скелет;
- Сопряженную замкнутую π-электронную систему, охватывающую все атомы цикла и содержащую 4n + 2, где n = 0, 1, 2, 3 и т.д. Эта формулировка известна, как правило Хюккеля. Критерии ароматичности позволяют отличать сопряженные ароматические системы от всех других. Бензол содержит секстет π-электронов и соответствует правилу Хюккеля при n = 1.

Что дает ароматичность:
Несмотря на высокую степень ненасыщенности, ароматические соединения устойчивы к действию окислителей и температуры, они более склонны вступать в реакции замещения, а не присоединения. Эти соединения обладают повышенной термодинамической стабильностью, обеспечивающейся высокой энергией сопряжения ароматической системы кольца (150 кДж/моль), поэтому арены предпочтительней вступают в реакции замещения, в результате чего сохраняют ароматичность.
Механизм реакций электрофильного замещения в ароматическом кольце:
Электронная плотность π-сопряженной системы бензольного кольца является удобным объектом для атаки электрофильными реагентами.
Как правило, электрофильные реагенты генерируются в процессе реакции при помощи катализаторов и соответствующих условий.
Е – Y → E δ + – Y δ - → E + + Y -
Образование π-комплекса. Первоначальная атака электрофилом π-электронного облака кольца приводит к координации реагента с π-системой и образованию комплекса донорно-акцепторного типа называемого π-комплекса. Ароматическая система не нарушается:

Образование σ-комплекса. Лимитирующая стадия, на ней электрофил образует ковалентную связь с атомом углерода за счет двух электронов π-системы кольца, что сопровождается переходом данного атома углерода из sp 2 - в sp 3 - гибридное состояние и нарушением ароматической, молекула превращается в карбокатион.

Стабилизация σ-комплекса. Осуществляется путем отщепления от σ-комплекса протона с помощью основания. При этом за счет двух электронов разрывающейся ковалентной связи С – Н восстанавливается замкнутая π-системы кольца, т.е. происходит возврат молекулы в ароматическое состояние:

Влияние заместителей на реакционную способность и ориентацию электрофильного замещения
Заместители в бензольном кольце нарушают равномерность в распределении π- электронного облака кольца и тем самым оказывают влияние на реакционную способность кольца.
- Электронодонорные заместители (Д) повышают электронную плотность кольца и увеличивают скорость электрофильного замещения, такие заместители называют активирующими.
- Электроноакцепторные заместители (А) понижают электронную плотность кольца и уменьшают скорость реакции, называются дезактивирующими.
АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ , обширный класс органических соединений, характерной чертой которых являются: 1) циклическое строение и 2) особая система распределения сил сродства внутри молекулы, сообщающая циклу большую прочность. Простейшим веществом этого чрезвычайно богатого соединениями класса органической химии является бензол, основной углеродный скелет которого схематически изображается в виде шестиугольника - «ядра». К ароматическим соединениям относят не только производные бензола и его гомологов, но также и конденсированные системы типа нафталина, фенантрена, хризена и т. д., составленные из двух, трех, четырех и т. д. ядер бензола, равно как и многие гетероциклические соединения, обладающие ароматическим характером, т. е. комплексом определенных специфических свойств. Свойства, отличающие ароматические соединения от жирных и алициклических:
1) Атомы водорода обладают большой подвижностью, что проявляется в способности ароматических соединений входить в различного рода реакции замещения. Особенно характерными являются химические превращения, протекающие при действии азотной и серной кислот. При этом происходит нитрование или сульфирование ароматических соединений, т. е. процессы, связанные с обменом атома (или атомов) водорода на нитро-группу NО 2 или сульфо-группу SО 3 H:
Обе эти реакции широко используются в технологии органических веществ.
2) Различные реакционные группы в ароматических соединениях по некоторым своим свойствам значительно отличаются от свойств этих же групп в соединениях жирного ряда: галоиды в галоидных производных бензола обладают меньшей реакциеспособностью по сравнению с галоидными алкилами; для обмена галоида в галоидных арилах (арил - ароматический углеводородный остаток) на другие группы (гидроксил, амино-группу и т. д.) приходится прибегать к более сильным химическим воздействиям, чем в соответствующих алифатических соединениях; щелочные свойства ароматических аминов значительно слабее аминов жирных. Этот «кислый» или «отрицательный» характер ароматического остатка находит свое отражение также в ряде других свойств ароматических соединений. Особенно резко отличаются ароматические амины своим отношением к азотистой кислоте; с ней они дают т. н. диазосоединения, аналоги которых в жирном ряду известны только в исключительных случаях. Изменение свойств гидроксила в ароматических соединениях выражается в повышении его кислотности; поэтому гидроксильные производные бензола – фенолы - обладают свойствами настоящих кислот. Они реагируют с водными растворами едких щелочей, образуя солеобразные соединения - феноляты. Дигидроксильные производные бензола, нафталина и т. д. обладают свойством при окислении, отнятием двух атомов Н, превращаться в своеобразные соединения - хиноны.
3) Главное отличие ароматических соединений от алифатических, и в особенности от сходных с ними по строению углеродного скелета алициклических соединений, заключается в особом состоянии насыщенности ароматического цикла. Эта насыщенность сообщает ароматическим соединениям чрезвычайную прочность и стойкость по отношению к различным химическим воздействиям. Эмпирические формулы ароматических углеводородов (С 6 Н 6 , С 7 Н 8 , С 10 Н 8 , С 14 Н 8 и т. д.) показывают, что эти соединения д. б. отнесены к классу ненасыщенных, характеризующихся реакциями присоединения и окисления. Между тем в этом отношении ароматических соединений обнаруживают существенные отличия. Бромистый водород, обычно легко присоединяющийся в месте двойной (этиленовой) связи, к ароматическим соединениям не присоединяется. Присоединение брома - одна из самых употребительных реакций на двойную связь - осуществляется в отношении ароматических соединений только при наличии особых условий. Особенно характерна устойчивость ароматического «ядра» к окислителям. В то время как жирные и алициклические ненасыщенные углеводороды быстро реагируют с марганцевокислым калием с образованием кислот, бензол в тех же условиях почти не изменяется. Если же при ядре ароматического соединения находится боковая цепь, как, например, в этилбензоле (С 6 Н 5 ·СН 2 ·СН 3), то последняя окисляется в карбоксильную группу, и полученное в результате соединение (бензойная кислота С 6 Н 5 ·СООН) сохраняет основной углеродный скелет ароматического соединения - свое ядро. Даже при сильных химических воздействиях, например при сплавлении с щелочами, циклы исходных соединений остаются неизменными.
Для объяснения своеобразных свойств ароматических соединений был предложен целый ряд различных теорий. Первая формула строения бензола была дана немецким химиком Кекуле (в 1865 г.). В структурной формуле Кекуле - 6 расположенных в виде шестиугольника метиновых групп (= СН-), из которых каждая связана с соседними одной двойной (этиленовой) связью и одной простой (формула I). В виду того, что этиленовые связи характеризуются вполне определенными химическими свойствами, которых ароматические соединения лишены, эта формула нуждалась в некоторых дополнительных гипотезах.

Одной из них явилась гипотеза парциальных валентностей Тиле, по которой остаточные силы химического сродства атомов углерода взаимно насыщаются, образуя замкнутую систему, где три двойные связи находятся в «конъюгации» - взаимном сопряжении (формула II). С развитием учения о природе химических сил, гл. обр. в связи с теорией Вернера, представления о строении бензола подвергались некоторым видоизменениям. По Вернеру, силы химического сродства углерода не представляют собой отдельных, независимо друг от друга действующих сил (единицы сродства), но являются частичным выражением одной силы - общего запаса сродства, заложенного в атоме углерода. Т. о. значение каждой данной валентности заранее не определено, но зависит от состояния насыщенности углеродного атома, т. е. от количества сродства, потраченного на насыщение другими атомами или группами. При циклическом строении молекулы подобное насыщение может происходить не только за счет связывания других, не входящих в цикл, атомов, но иногда осуществляется внутренним распределением сродства между теми атомами, из которых данный цикл составлен. В бензоле этому способствует шестичленная симметричная структура, благодаря которой остаточное сродство каждого из шести атомов углерода приходит в состояние внутреннего насыщения, сообщающего циклу большую прочность и устойчивость. Подобные представления о строении бензола находят свое выражение в формуле III, где дугообразные связи иллюстрируют характер внутреннего циклического насыщения. В последнее время, в связи с учением о строении атома, были предложены новые электронные формулы строения бензола и других ароматических соединений, однако до сих пор они не получили широкого распространения в органической химии и являются только б. или м. удачной попыткой объяснения свойств ароматических соединений, как результата действия электростатических сил.
Главным источником получения ароматических соединений является каменноугольная смола - продукт сухой перегонки каменного угля. В результате ее обработки, состоящей из различных операций физического и химического характера, добываются разнообразные ароматические соединения, составляющие основу производства красителей, фармацевтических препаратов, взрывчатых, душистых и многих других веществ. Важнейшими ароматическими соединениями каменноугольной смолы являются бензол, толуол, ксилол, фенол, крезол, нафталин, фенантрен и антрацен, промышленная разработка которых в связи с планомерными научными исследованиями вызвала совершенно исключительный рост химической промышленности в конце прошлого и в начале нынешнего столетия.